FDA amplía aprobación de vacuna contra el VSR de Moderna: Ahora incluye a este grupo de personas
La decisión de incluir a personas menores de 60 años aún está pendiente.
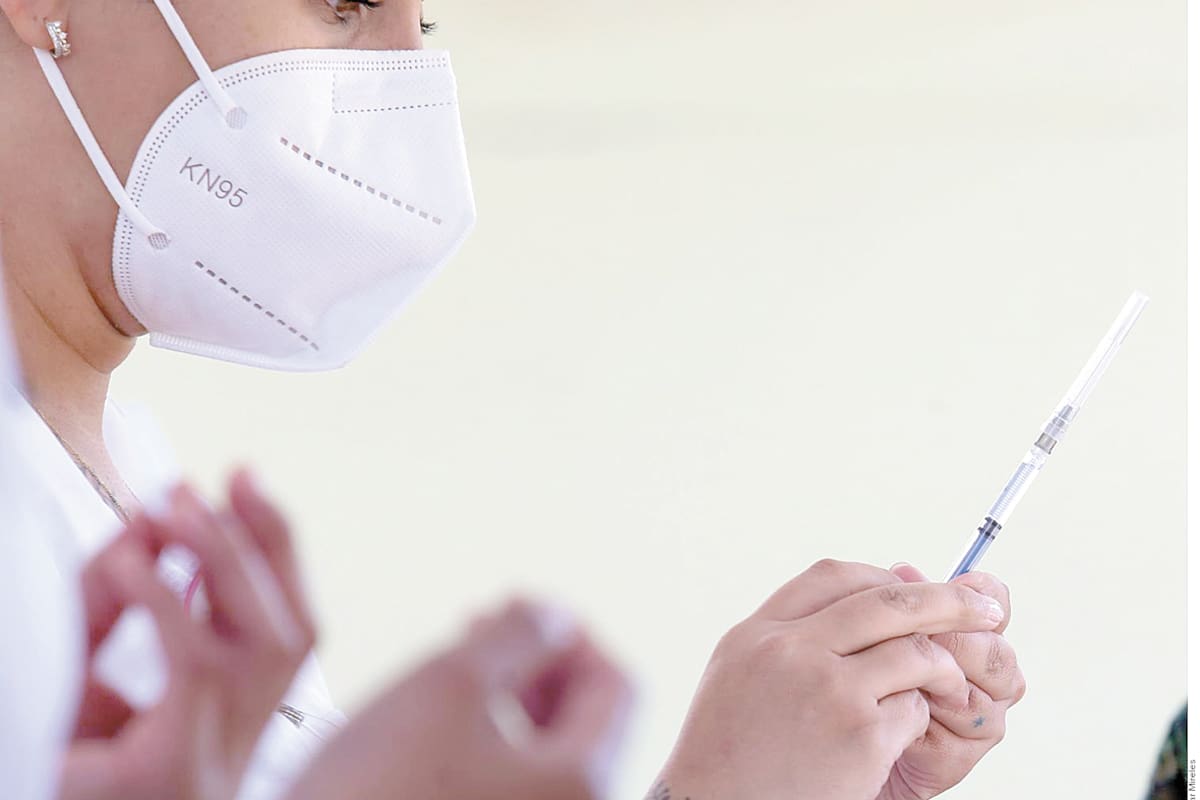
ESTADOS UNIDOS.- Este jueves, la Administración de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inglés) amplió la aprobación de la vacuna contra el virus respiratorio sincitial (VSR) desarrollada por Moderna para incluir a adultos menores de 60 años que presentan un mayor riesgo de desarrollar complicaciones por la enfermedad.
Anteriormente, la vacuna —conocida como mRESVIA— solo estaba autorizada para personas de 60 años o más, según ABC.
Esta ampliación se basó en los resultados de un ensayo clínico avanzado que demostró que el fármaco es eficaz para estimular la respuesta inmunitaria también en adultos más jóvenes con condiciones médicas crónicas.
Un riesgo grave para ciertos pacientes
“El VSR representa un grave riesgo para la salud de los adultos con ciertas enfermedades crónicas, y la aprobación de hoy marca un avance importante en nuestra capacidad para proteger a más poblaciones de enfermedades graves causadas por el VSR”, expresó Stéphane Bancel, director ejecutivo de Moderna, en un comunicado.
“Agradecemos la revisión de la FDA y agradecemos a todos los participantes en nuestro ensayo clínico, así como al equipo de Moderna, su dedicación para proteger a las personas contra el VSR”.
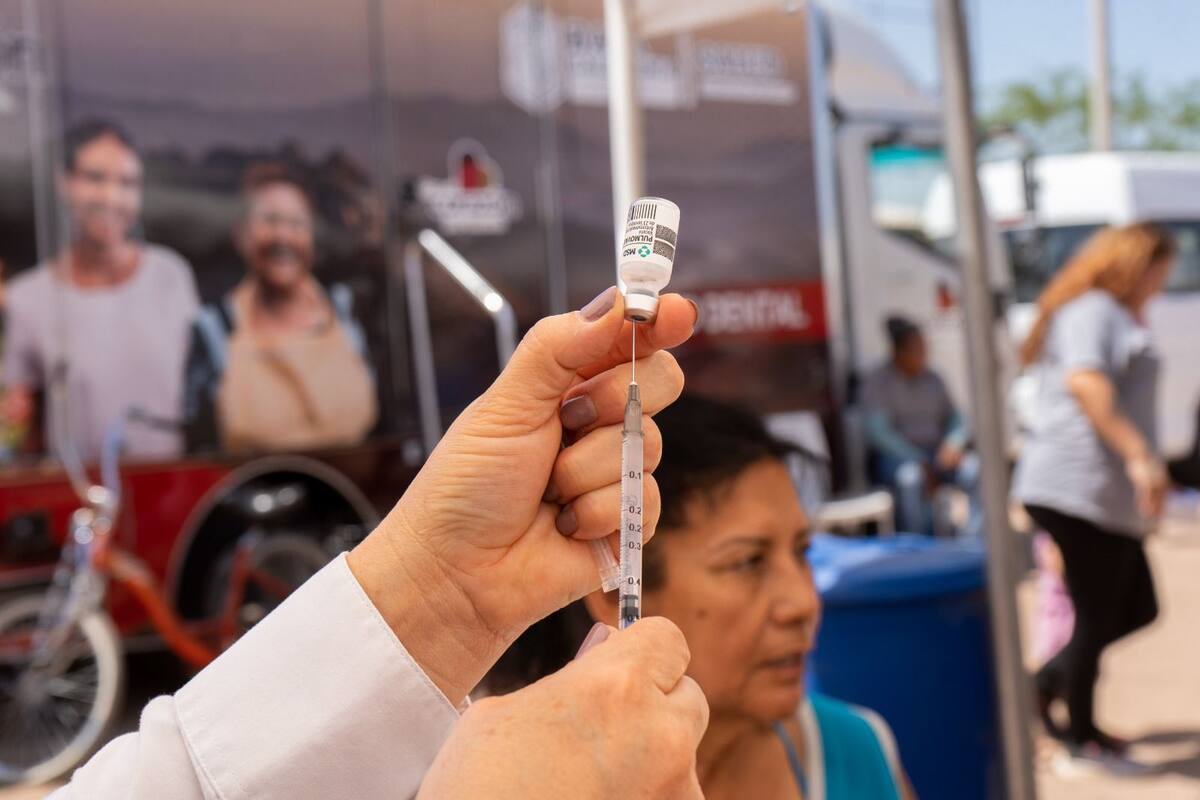
Vacunación aún limitada por recomendación de los CDC
Pese a la autorización de la FDA, los Centros para el Control y la Prevención de Enfermedades (CDC) son quienes establecen qué grupos deben recibir la vacuna y en qué momento.
Actualmente, los CDC recomiendan la vacunación contra el VSR únicamente para adultos de 75 años o más, y para aquellos de entre 60 y 74 años que padecen afecciones de alto riesgo.
La decisión de incluir a personas menores de 60 años aún está pendiente. El comité asesor independiente de vacunas de los CDC deberá votar para emitir una recomendación, que luego será evaluada por la dirección del organismo.
Cambios en el liderazgo y postergación de decisiones
La recomendación final podría demorarse, ya que el puesto de director de los CDC permanece vacante.
Desde abril, el secretario de Salud y Servicios Humanos, Robert F. Kennedy Jr., ha estado emitiendo decisiones finales sobre políticas de vacunación.
A principios de esta semana, Kennedy destituyó a los 17 miembros del comité asesor en funciones y los reemplazó con ocho nuevos integrantes.
Te puede interesar: Docentes, personal de guarderías y trabajadores de salud serán vacunados contra el sarampión
En una reunión previa celebrada en abril, el comité anterior había votado a favor de recomendar la vacunación para adultos de entre 50 y 59 años con condiciones de riesgo. Sin embargo, Kennedy decidió no adoptar esa sugerencia.
Se espera que el nuevo comité vuelva a discutir esta y otras vacunas —incluidas las de VPH y COVID-19— durante su próxima reunión del 25 al 27 de junio. Varios de los nuevos miembros han manifestado escepticismo sobre el uso de tecnología de ARNm, base sobre la cual se desarrolló mRESVIA.
Baja cobertura de vacunación
A pesar de la disponibilidad de la vacuna, la cobertura entre las poblaciones objetivo ha sido baja.
Según datos de los CDC actualizados al 26 de abril, solo el 47.5 % de los adultos de 75 años o más y el 38.1 % de los adultos de 60 a 74 años con una condición de alto riesgo habían recibido al menos una dosis de la vacuna contra el VSR.
Sigue nuestro canal de WhatsApp
Recibe las noticias más importantes del día. Da click aquí

 Grupo Healy © Copyright Impresora y Editorial S.A. de C.V. Todos los derechos reservados
Grupo Healy © Copyright Impresora y Editorial S.A. de C.V. Todos los derechos reservados